| Comenzado el | martes, 13 de junio de 2017, 11:59 |
|---|---|
| Estado | Terminado |
| Finalizado en | martes, 13 de junio de 2017, 12:02 |
| Tiempo empleado | 3 minutos |
| Puntos | 6/6 |
| Calificación | 10 de un total de 10 (100%) |
Esta es una página creada para consulta en ningún momento debe de ser usada para otra cosa DI NO AL PLAGIO, en caso de querer contactar sobre alguna tarea para mayor orientación HAGANLO EN EL CORREO, con gusto les atenderé en comentarios no siempre puedo contestar.
Mostrando las entradas con la etiqueta Modulo 12. Mostrar todas las entradas
Mostrando las entradas con la etiqueta Modulo 12. Mostrar todas las entradas
martes, 13 de junio de 2017
Modulo 12 Semana 4 Conceptos de electricidad y magnetismo
Ley de Avogadro
Concepto de MOL
 El número de átomos
en 1 mol de cualquier elemento se llama el número de Avogadro que es: 6.022 x
1023.
El número de átomos
en 1 mol de cualquier elemento se llama el número de Avogadro que es: 6.022 x
1023.
1 mol de cualquier elemento es una muestra del elemento con
su masa en gramos es igual a la masa atómica de ese elemento.
Esta ley, descubierta por Avogadro a principios del siglo
XIX, establece la relación entre la cantidad de gas y su volumen cuando se
mantienen constantes la temperatura y la presión. La cantidad de gas será
considerada en moles.
 Ley de Avogadro
Ley de Avogadro
“El volumen de un gas es directamente proporcional a la
cantidad de materia (número de moles), a presión y temperatura constantes”.
Entonces la Ley de
Avogadro para un cambio de condiciones iniciales a condiciones finales es:
Ejemplo:
Sabemos que 3.50 L de un gas contienen 0.875 mol. Si
aumentamos la cantidad de gas hasta 1.40 mol, ¿cuál será el nuevo volumen del
gas? (a temperatura y presión constantes).
Usemos la expresión de la ley de
Avogadro
|
|
Despejemos los valores que estamos
buscando
|
|
Sustituyamos los valores
|
|
Multiplicamos los valores del numerador
|
|
Dividiendo
|
|
Simplifiquemos las unidades
|
|
El volumen final
|
|
lunes, 12 de junio de 2017
Ley de Charles
La unidad en el Sistema Internacional de Medidas (SI) para
el volumen es el m3 y la
temperatura se maneja en kelvin.
Ley de Charles
“A presión constante, el volumen
de la masa de un gas es directamente proporcional a la temperatura absoluta
del gas”
|
|
Si tenemos un volumen de gas, que
se encuentra a una temperatura (T1) y variamos el volumen de gas
hasta (V2), entonces la temperatura cambiará (T2)
|
Expresión algebraica.
|
Ejemplo:
Un gas tiene un volumen de 2.5 L a 25°C. ¿Cuál será su nuevo
volumen si bajamos la temperatura a 10°C?
·
Primero expresamos la temperatura en kelvins.
T1= 25°C + 273.15 = 298.15K
T2= 10°C + 273.15 = 283.15K
·
Usamos la expresión
·
Sustituyamos la presión y temperatura iniciales
V1, T1 y la temperatura final T2
·
Multiplicamos los valores del numerador.
·
Dividamos los valores restantes.
·
Simplifiquemos las unidades.
·
Volumen final después del cambio de temperatura.
V2
= 2.37l
Ley de Gay-Lussac
Ley de Gay-Lussac
 Enunciada por Gay-Lussac a principios de 1800, en la que establecía
la relación entre la temperatura y la presión de un gas cuando el volumen es
constante.
Enunciada por Gay-Lussac a principios de 1800, en la que establecía
la relación entre la temperatura y la presión de un gas cuando el volumen es
constante.Se puede aumentar la presión del gas añadiendo calor al recipiente, siempre y cuando el volumen sea constante. |
al añadir calor, la presión del gas aumenta ya que las moléculas de este chocan a una mayor velocidad en el mismo volumen que se encontraba anteriormente. |
|
|
EJEMPLO.
Un gas recibe una presión de 3atm, su temperatura es de 280K
y ocupa un volumen de 3.5cm3. Si el volumen es constante y la
temperatura aumenta a 310K ¿Cuál es ahora la presión del gas?
Despejemos la presión final de P2
|
|
Sustituyamos la presión y
temperatura iniciales P1, T1 y la temperatura final T2
|
|
Multipliquemos los valores del
numerador
|
|
Dividamos los valores
|
|
Simplifiquemos las unidades
|
|
Esta es la presión del gas cuando
la temperatura aumento
|
|
Ley de Boyle-Mariotte
Las primeras mediciones experimentales del comportamiento
térmico de los gases fueron realizadas por Robert Boyle (1627-1691). Él llevó a
cabo un estudio exhaustivo de los cambios en el volumen de los gases como
resultado de cambios en la presión. Las demás variables, como la masa y la
temperatura, se mantuvieron constantes.
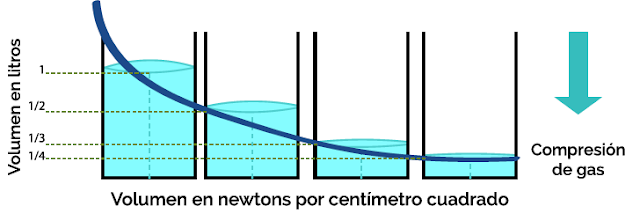
Boyle encontró que cuando la presión se disminuye a la
mitad, el volumen se duplica, es decir, que existe una variación proporcional
inversa entre las dos cantidades.
Sus resultados fueron llamados:
Ley de Boyle
“A temperatura constante, el volumen
de una masa gaseosa es inversamente proporcional a la presión que se aplica.”
Tenemos un volumen de gas V₁ que se
encuentra a una presión P₁. Si variamos el volumen de gas hasta V₂, entonces la
presión cambiará a P₂.
P₁ V₁ = P₂
V₂
Ejemplo
¿Qué volumen de gas hidrógeno a presión atmosférica se
requiere para llenar un tanque de 5000cm3 bajo una presión de 530 Pa ?
Primero identifiquemos las condiciones iniciales y las
condiciones finales. Las condiciones iniciales serán la presión atmosférica,
cuyo valor es 101325 Pa, y el volumen de gas hidrógeno que estamos buscando.
Las condiciones finales serán el volumen del tanque y la presión que este
posee.
|
|
Tomemos
la expresión de la ley de Boyle
|
|
|
Despejemos
el volumen inicial
|
|
|
Sustituyamos
valores
|
|
|
Multipliquemos
las cantidades del numerador
|
|
|
Dividamos
los valores
|
|
|
Simplifiquemos
unidades
|
|
|
Volumen
de hidrógeno buscado
|
Suscribirse a:
Entradas (Atom)
¿Qué es la administración?
Hablar de administración abarca desde antes de nuestra era, filósofos como Sócrates, Platón y Aristóteles la han incluido en sus disc...
-
Mezcla es una combinación formada por dos o más componentes en la cual las partes que la forman no reaccionan químicamente entre sí, por lo ...
-
Un bioma (del griego “ bios ” = vida) es un área determinada que comparte un clima, una flora y una fauna característica. Un bioma es un con...
-
Introducción Hay tres preposiciones de tiempo básicas en ingles: at, in, on . La utilización de estas preposiciones tiene algunas regla...